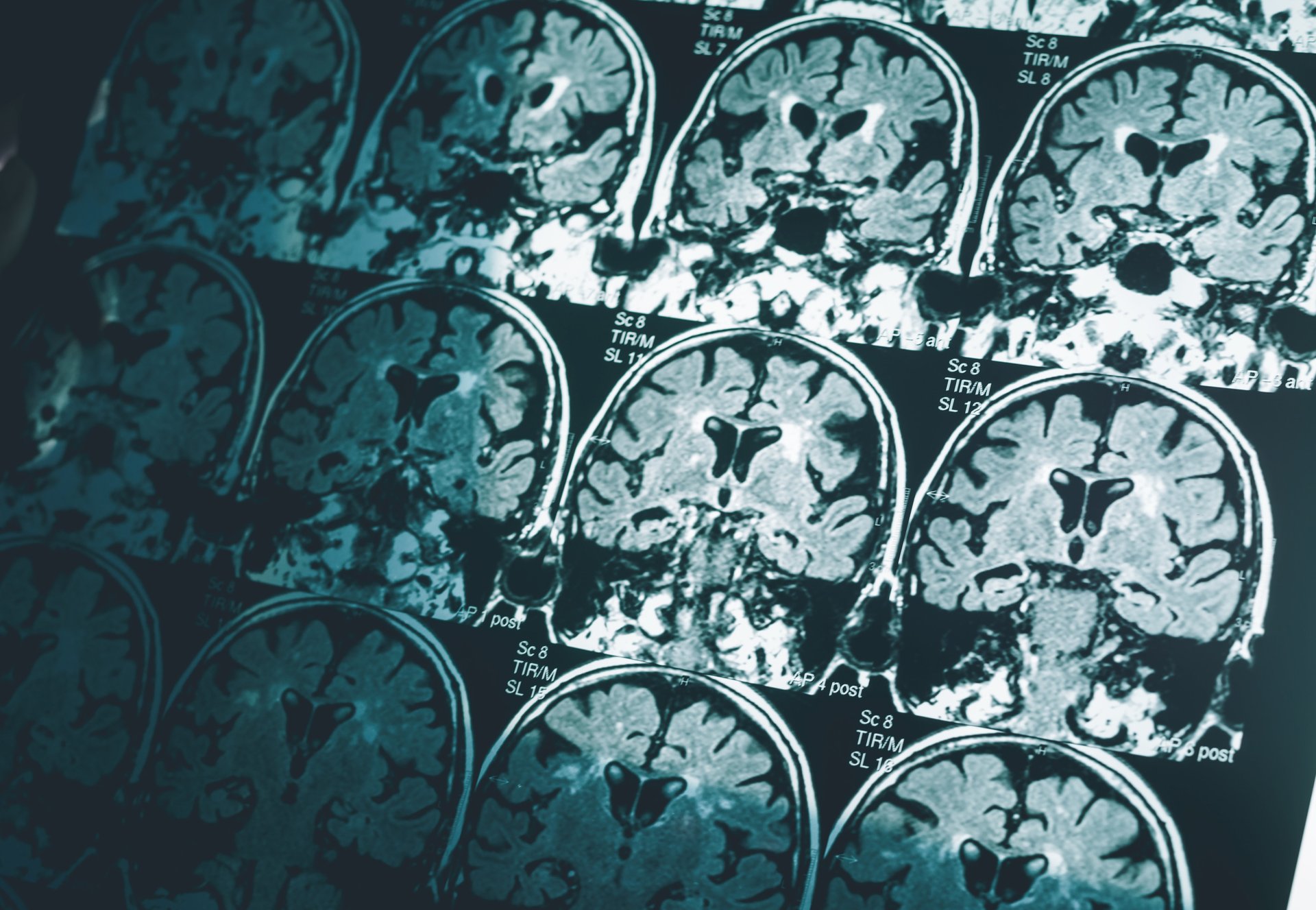
¿Un tratamiento para revertir el Alzheimer? El éxito de los modelos celulares, sus implicaciones y perspectivas futuras
La enfermedad de Alzheimer es una enfermedad neurodegenerativa que aún presenta incógnitas en cuanto a sus causas. Sin embargo, estudios recientes han identificado una serie de factores que pueden desempeñar un papel importante en su desarrollo. Examinaremos el papel de CDK5 en la patogénesis de la enfermedad de Alzheimer y se explorará los avances terapéuticos en la modulación de la actividad de CDK5 para mitigar los síntomas de la enfermedad.
NEUROLOGÍAMEDICINAINNOVACIÓN
¿Qué es la enfermedad de Alzheimer?
El Alzheimer es un trastorno neurológico que afecta el cerebro, lo que conduce a una disminución progresiva de la memoria, la capacidad de pensamiento y el comportamiento. Actualmente es la causa más común de demencia según el Instituto Nacional de Salud (NIH)
Brian Oleksiw 2019 for Jox. What are the early signs of Alzheimer's and am I at risk?.


Algunos síntomas tempranos de la enfermedad de Alzheimer incluyen:
Tener dificultad para recordar eventos recientes.
Tener problemas para completar tareas familiares y extraviar artículos.
Progresivamente, estos síntomas empeoran y el individuo experimenta:
Confusión
Pérdida de memoria
Dificultad para comunicarse
Fuertes cambios de humor
En última instancia, la enfermedad de Alzheimer hace que los afectados sean incapaces de completar la tarea más simple.
¿Cuáles son los síntomas tempranos del Alzheimer?
Foto de Road Trip with Raj en Unsplash
¿Por qué se presenta la enfermedad de Alzheimer?
Todavía se está determinando. Pero actualmente se ha identificado una serie de factores principales que intervienen en el desarrollo de la enfermedad.
Algunos de los factores más importantes son:
La aceleración del envejecimiento
La genética
Los factores ambientales


Foto de Sangharsh Lohakare en Unsplash

Existe una enzima identificada como quinasa dependiente de ciclina 5 (CDK5) que es muy común en el cerebro ya que está involucrada en varios procesos celulares:
La migración neuronal
La función sináptica
La supervivencia neuronal
Estudios han revelado que CDK5 puede influir en la formación de ovillos de tau y placas amiloides, dos características patológicas distintivas de la enfermedad de Alzheimer.
Foto de Natasha Connell en Unsplash
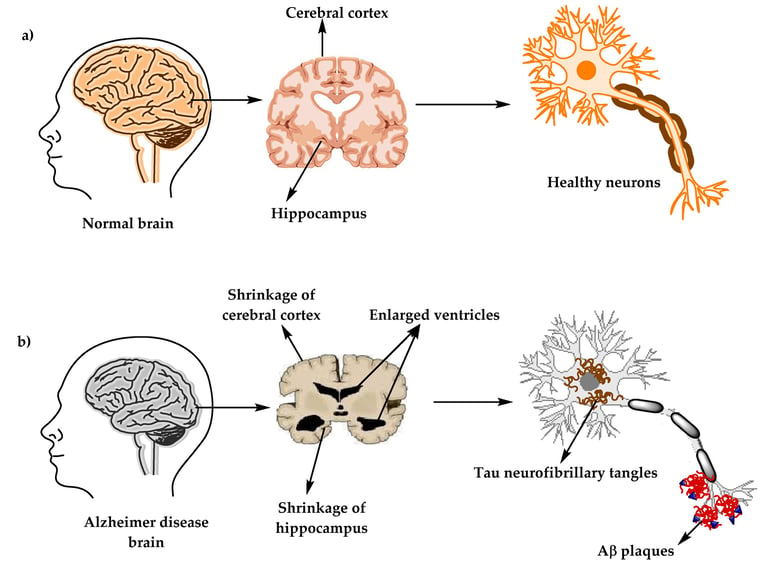
a) La estructura normal del cerebro y b) La estructura de un cerebro con la enfermedad de Alzheimer. Breijyeh, Z., & Karaman, R. (2020). Comprehensive review on Alzheimer’s disease: causes and treatment.
La fosforilación anormal de la proteína tau por CDK5 puede promover la acumulación de ovillos de tau en el cerebro. Esta fosforilación alterada hace que la proteína tau sea más propensa a la formación de ovillos, que son agregados anormales asociados con la disfunción neuronal característica de la enfermedad de Alzheimer.
¿Cuáles son los avances terapéuticos para tratar el Alzheimer?
Los investigadores han explorado enfoques terapéuticos dirigidos a modular la actividad de CDK5 como una estrategia potencial para tratar la enfermedad de Alzheimer. Un estudio reciente realizado por el equipo del MIT utilizó un péptido diseñado para inhibir la actividad de CDK5 en modelos animales y en cultivos de células humanas. Los resultados fueron alentadores, ya que se observó una reducción de la patología y una protección contra la neurodegeneración asociada a las proteínas tau.
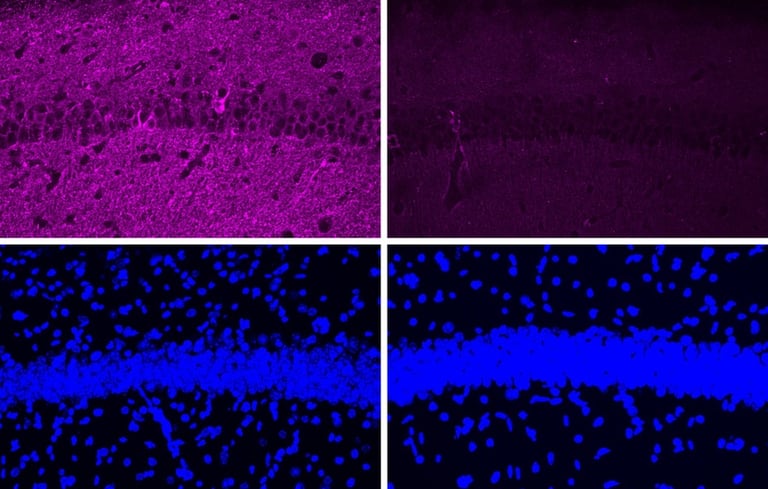
En los cerebros de los ratones tratados con el nuevo péptido (dos paneles de la derecha), se observan muchas menos proteínas Tau (teñidas de púrpura) en la parte superior derecha. Los paneles de la izquierda muestran neuronas de ratones tratados con una versión codificada del péptido. En los dos paneles inferiores, el ADN de los núcleos celulares se tiñe de azul, lo que muestra que los cambios en los niveles de Tau no son causados por cambios significativos en la población celular. Crédito: Ping-Chieh Pao para MIT News
CDK5 y la patogénesis de la enfermedad de Alzheimer
Además, CDK5 también está involucrada en el procesamiento de la proteína precursora de amiloide (APP), cuya acumulación da lugar a placas amiloides en el cerebro. La fosforilación de APP por CDK5 puede contribuir a su escisión en péptidos beta-amiloides, lo que a su vez promueve la formación de placas amiloides.
Además, este tratamiento también mostró efectos protectores contra la neurodegeneración en modelos animales, mejorando los déficits conductuales relacionados con la hiperactividad de CDK5.
¿Se podrá en un futuro curar la enfermedad de Alzheimer?
La enfermedad de Alzheimer es un trastorno complejo con múltiples factores que contribuyen a su desarrollo. Los avances en la comprensión de la patogénesis de la enfermedad identificando a CDK5 como un jugador importante en la acumulación de proteína tau y placas amiloides promete bastante, pero es un inicio.


Foto de Johnny Cohen en Unsplash
Los enfoques terapéuticos dirigidos a modular la actividad de CDK5 han demostrado efectos prometedores en la reducción de la patología y la protección contra la neurodegeneración. Estos hallazgos abren nuevas perspectivas para el desarrollo de tratamientos dirigidos a CDK5 como una estrategia terapéutica potencial en la enfermedad de Alzheimer. Sin embargo, aún queda mucho por investigar y se requieren estudios adicionales para comprender completamente el papel de CDK5 en la enfermedad y optimizar las intervenciones terapéuticas.


Foto de Louis Reed en Unsplash
Los procesos neurodegenerativos pueden desencadenar la acumulación de calcio en las neuronas, lo que activa una proteasa llamada calpaína.
La calpaína y la patogénesis de la enfermedad de Alzheimer


La calpaína, a su vez, corta una porción N-terminal de la proteína p35, liberando los fragmentos p25. Tanto p35 como p25 pueden activar la quinasa dependiente de ciclina 5 (CDK5). La activación a través de p35 permite que CDK5 tenga una vida media más larga en comparación con la activación directa por p25. Además, se ha descubierto que la calpaína libera indirectamente CDK5 activada con p35 o p25 desde los sitios de la membrana. Los científicos sospecharon que la presencia prolongada de esta proteína en el medio extracelular es responsable del aumento de la fosforilación de las proteínas tau que causan la patología de la enfermedad de Alzheimer. Entonces, propusieron generar una p35 no escindible por calpaína (p35 transgénica) a través de manipulación genética en ratones.
Foto de Johnny Cohen en Unsplash